Przez wieki medycyna patrzyła na bakterie jednym okiem — tym podejrzliwym. Drobnoustroje kojarzyły się z zarazą, epidemiami i brudem, który trzeba wyeliminować. Antybiotyki stały się jednym z największych triumfów XX-wiecznej farmakologii i słusznie, bo uratowały miliony istnień. Tyle że przy okazji przyzwyczaiły nas do myślenia, że każdy mikrob to wróg. A prawda okazała się znacznie bardziej skomplikowana.
Od mniej więcej dwóch dekad nauka odkrywa na nowo to, o czym Ilja Miecznikow — rosyjski noblista — intuicyjnie przeczuwał już na początku XX wieku: że pewne bakterie mogą nam pomagać. Miecznikow obserwował bałkańskich pasterzy dożywających sędziwego wieku na diecie obfitej w fermentowane mleko i podejrzewał, że żyjące w nim pałeczki kwasu mlekowego odgrywają tu jakąś rolę. Nie miał narzędzi, żeby to udowodnić. My — wreszcie mamy.
Ile nas właściwie jest?
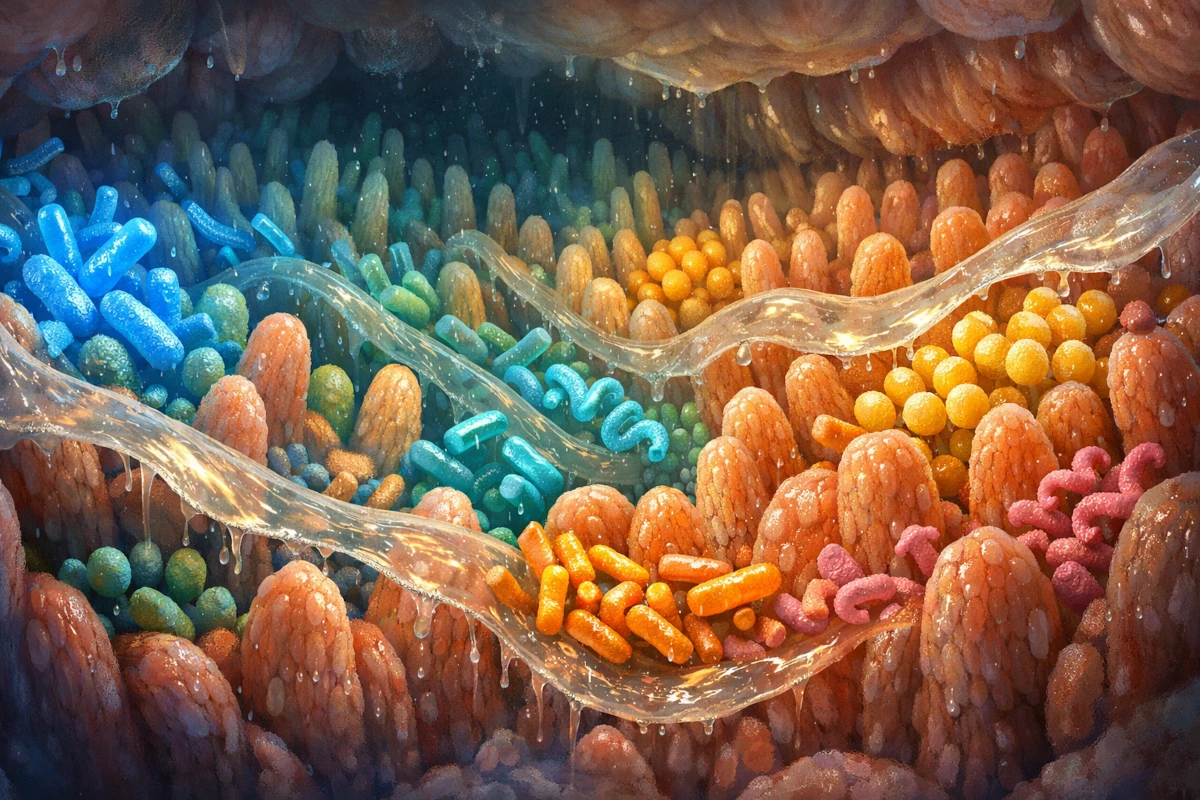
Przez lata powtarzano chwytliwą statystykę: na jedną komórkę ludzką przypada dziesięć bakteryjnych, więc w gruncie rzeczy jesteśmy bardziej bakterią niż człowiekiem. Brzmiało efektownie, ale okazało się mocno przesadzone. W 2016 roku Ron Sender, Shai Fuchs i Ron Milo z Instytutu Weizmanna opublikowali w PLOS Biology skrupulatne przeliczenie. Wyszło im, że dorosły mężczyzna o wadze 70 kilogramów nosi w sobie około 38 bilionów komórek bakteryjnych przy 30 bilionach komórek własnych — stosunek bliższy 1,3 do 1 niż mitycznemu 10 do 1. Łączna masa tych bakterii to jakieś 200 gramów, mniej więcej tyle co kostka masła.
Liczby robią wrażenie, choć mniejsze niż dawniej. Ale o wadze mikrobiomu — tak naukowcy nazywają zbiorczą pulę genów wszystkich naszych mikrobów — nie decyduje liczba komórek, lecz to, co te komórki potrafią. Ludzki genom zawiera około 20 tysięcy genów kodujących białka. Mikrobiom dokłada do tej puli kolejne 2–3 miliony unikalnych genów. To tak, jakby każdy z nas nosił dodatkową, ogromną apteczkę molekularną, która produkuje substancje, do których nasz własny organizm nie ma przepisu.
Krótkie łańcuchy, długie konsekwencje
Gdyby zapytać gastroenterologa, co najważniejszego robią bakterie jelitowe, prawdopodobnie usłyszelibyście jeden magiczny skrótowiec: SCFA, czyli krótkołańcuchowe kwasy tłuszczowe. Chodzi o trzy o trzy związki: maślan, propionian i octan. Powstają, gdy bakterie z grupy Firmicutes fermentują błonnik pokarmowy — ten sam, którego sami strawić nie potrafimy.
Maślan jest tu gwiazdą. Stanowi główne źródło energii dla kolonocytów, czyli komórek wyściełających jelito grube. Bez niego nabłonek jelitowy słabnie, a bariera ochronna między światłem jelita a krwioobiegiem staje się nieszczelna. Ale maślan to nie tylko paliwo. Badania wykazały, że hamuje on aktywność deacetylaz histonów (HDAC) — enzymów uczestniczących w regulacji ekspresji genów. W praktyce oznacza to, że maślan wpływa na to, które geny w komórkach jelita są włączone, a które wyłączone. Między innymi dlatego niskie stężenia maślanu wiążą się ze zwiększonym ryzykiem nowotworów jelita grubego — komórki tracą jeden z mechanizmów kontrolujących ich niekontrolowany wzrost.
Propionian i octan grają inne role. Propionian trafia do wątroby i uczestniczy w regulacji gospodarki glukozowej. Octan krąży w krwiobiegu i dociera do mózgu, gdzie wpływa na poczucie sytości.
Trzy proste kwasy. Dwieście gramów bakterii. I nagle okazuje się, że każdy posiłek to negocjacja między nami, a nimi.
Kiedy bariera pęka
Co się dzieje, gdy bakterie jelitowe nie dostają błonnika? Na to pytanie odpowiedzieli w 2016 roku Mahesh Desai i Eric Martens z Uniwersytetu Michigan w głośnym badaniu opublikowanym w Cell. Wykorzystali myszy skolonizowane syntetyczną mikrobiotą ludzką i karmili je dietą pozbawioną włókien roślinnych. Wyniki były alarmujące.
Bakterie, pozbawione błonnika jako źródła pożywienia, zaczęły trawić coś innego — warstwę śluzu pokrywającą ściany jelita. Śluz jelitowy to bariera zbudowana głównie z glikoproteiny mucyny 2 (MUC2), która fizycznie oddziela drobnoustroje od nabłonka. Gdy bakterie, zwykle wyspecjalizowane w rozkładzie polisacharydów roślinnych, przerzuciły się na degradację mucyn, warstwa ochronna dramatycznie zmniejszyła się. W konsekwencji myszy stały się podatne na zakażenie Citrobacter rodentium — patogenem modelowym imitującym ludzkie zakażenia E. coli. U myszy karmionych dietą bogatą w błonnik ten sam patogen nie stanowił poważnego zagrożenia.
Badanie Desaia i Martensa dostarczyło jednego z najjaśniejszych mechanistycznych wyjaśnień tego, dlaczego diety ubogie w warzywa, owoce i produkty pełnoziarniste — typowe dla zachodniego stylu żywienia — mogą sprzyjać chorobom jelit, w tym nieswoistym zapaleniom jelit (IBD). Nasze bakterie, gdy nie mają co jeść, zaczynają dosłownie zjadać nas od środka.
Pierwsze godziny, które decydują o latach
Ale cofnijmy się do samego początku. Do momentu, w którym nasz mikrobiom zaczyna się formować — bo to, co się wtedy wydarzy, rzutuje na resztę życia.
Skład mikrobioty jelitowej nie jest dziełem przypadku. Kształtuje się w dużej mierze w pierwszych miesiącach i latach życia, a sposób przyjścia na świat ma tu zaskakująco duże znaczenie. Noworodek rodzący się drogami natury przechodzi przez kanał rodny matki, gdzie zostaje skolonizowany jej bakteriami pochwy i jelit — to swoisty „pakiet startowy", ewolucyjnie dopasowany do potrzeb nowego organizmu. Dziecko urodzone przez cesarskie cięcie omija ten etap i jest kolonizowane przede wszystkim bakteriami skóry matki oraz środowiska szpitalnego, co skutkuje innym, zwykle mniej zróżnicowanym profilem mikrobioty we wczesnym okresie życia.
Karmienie piersią dokłada kolejny element układanki. Mleko kobiece zawiera nie tylko składniki odżywcze, ale też oligosacharydy (HMO) — złożone cukry, których niemowlę nie trawi. Trawieniem HMO zajmują się natomiast określone gatunki Bifidobacterium, dla których oligosacharydy te stanowią swego rodzaju wybiórczy pokarm. To elegancki ewolucyjny mechanizm: matka karmi bakterie, które powinny kolonizować jelito jej dziecka.
Te wczesne doświadczenia mikrobiologiczne mają konsekwencje wykraczające daleko poza okres niemowlęcy. Tak zwana hipoteza higieniczna — a dokładniej jej nowsza wersja, hipoteza „starych przyjaciół" — głosi, że ograniczony kontakt z różnorodnymi mikroorganizmami we wczesnym dzieciństwie zwiększa ryzyko chorób autoimmunologicznych, alergii i astmy w późniejszym życiu. Układ odpornościowy, pozbawiony odpowiednich „partnerów treningowych" w postaci nieszkodliwych drobnoustrojów, może reagować nadmiarowo na nieszkodliwe bodźce — pyłki, roztocza, białka pokarmowe. Badania epidemiologiczne konsekwentnie pokazują, że dzieci wychowywane na wsiach, w kontakcie ze zwierzętami gospodarskimi, chorują na alergie i astmę rzadziej niż ich rówieśnicy z miast. Nie chodzi oczywiście o to, żeby rezygnować z higieny — chodzi o zrozumienie, że pewien poziom ekspozycji na drobnoustroje jest organizmowi potrzebny.
Jelito rozmawia z mózgiem
Muszę tu poczynić osobiste wyznanie. Kiedy kilka lat temu natknęłam się na pierwsze doniesienia o tym, że bakterie jelitowe mogą wpływać na nastrój, pomyślałam: „No jasne, kolejny modny pseudonaukowy trend." Myliłam się. I to grubo.
Około 90–95% serotoniny w organizmie produkowane jest w jelitach. Nie w mózgu. Tak, trzeba to przeczytać dwa razy, bo łamie pewien intuicyjny schemat. Oczywiście serotonina jelitowa i mózgowa pełnią różne funkcje, a ta pierwsza nie przekracza bariery krew-mózg. Jednak bakterie jelitowe wpływają na jej syntezę, a sygnały z jelita docierają do ośrodkowego układu nerwowego przede wszystkim za pośrednictwem nerwu błędnego — najdłuższego nerwu czaszkowego, stanowiącego coś w rodzaju biologicznej autostrady łączącej brzuch z głową. Bakterie produkują też inne neuroaktywne substancje: kwas gamma-aminomasłowy (GABA), dopaminę czy noradrenalinę.
Z tego rozpoznania wyrosła koncepcja psychobiotyków — określonych szczepów bakteryjnych, które mogą korzystnie wpływać na zdrowie psychiczne. To nie są obietnice marketingowe z etykiet jogurtów. W 2011 roku Michaël Messaoudi i współpracownicy opublikowali w British Journal of Nutrition wyniki randomizowanego, podwójnie zaślepionego badania klinicznego z udziałem zdrowych ochotników. Kombinacja dwóch szczepów — Lactobacillus helveticus R0052 i Bifidobacterium longum R0175 — podawana przez 30 dni obniżyła wyniki w sposób mierzalny lęk, depresję i poziom odczuwanego stresu w porównaniu z placebo. Uczestnicy wykazywali też niższe stężenie kortyzolu w moczu.
Obiecujące wyniki przynoszą również badania nad szczepem Lactiplantibacillus plantarum PS128, testowanym między innymi wśród osób narażonych na chroniczny stres zawodowy. Trzeba jednak wyraźnie powiedzieć: psychobiotyki nie zastępują psychoterapii ani farmakoterapii. Są raczej potencjalnym elementem uzupełniającym, a dokładne dawkowanie i wskazania wymagają jeszcze wielu lat badań. Metaanalizy, choć zachęcające, konsekwentnie podkreślają heterogeniczność dotychczasowych prób klinicznych — różne szczepy, różne dawki, różne populacje badanych.
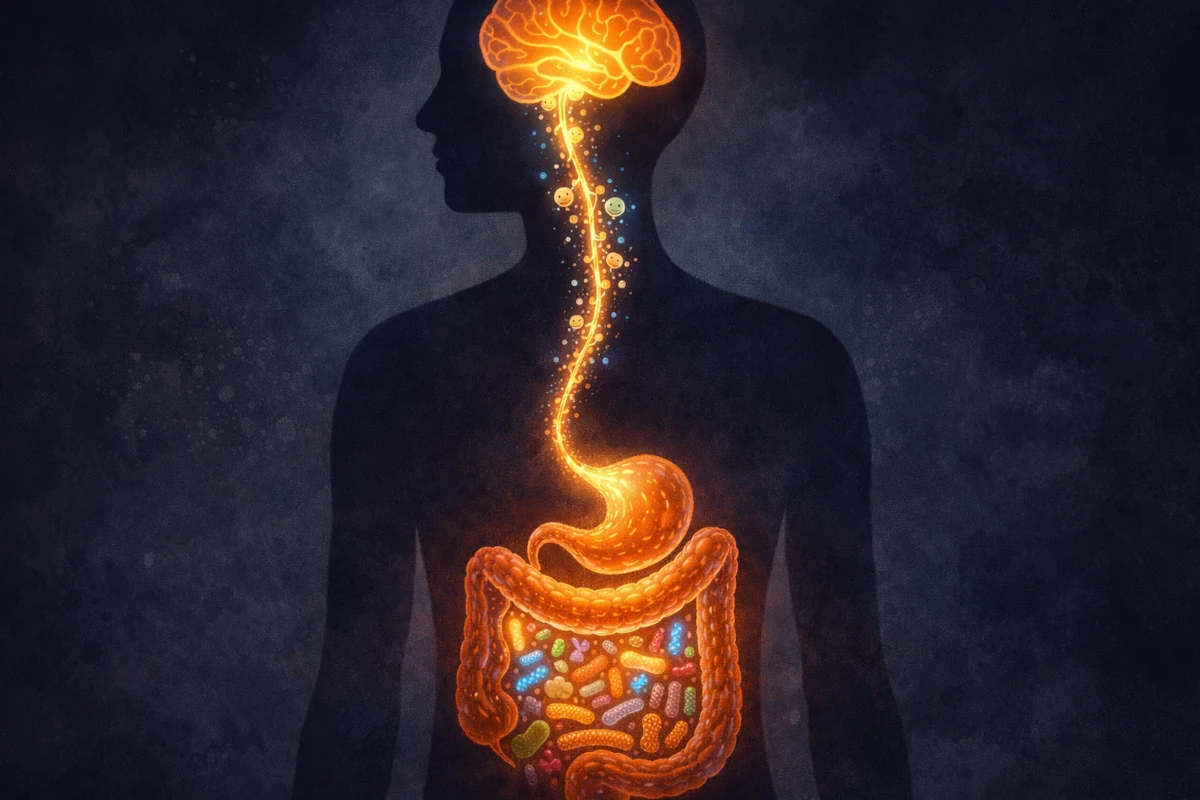
Wizualizacja AI / faleinspiracji.pl / CC BY 4.0
Twój chleb to nie mój chleb
Mikrobiota nie jest statyczna — reaguje na to, jak żyjemy. W 2014 roku zespół Siobhan Clarke z University College Cork zbadał mikrobiotę irlandzkich zawodowych rugbystów i porównał ją z dwiema grupami kontrolnymi dopasowanymi pod względem wieku. Jelita sportowców okazały się znacznie bardziej zróżnicowane pod kątem gatunków bakteryjnych niż jelita osób prowadzących siedzący tryb życia. Zróżnicowanie mikrobiomu to w tej dziedzinie parametr niemal zawsze kojarzony pozytywnie — im więcej gatunków, tym bardziej odporny ekosystem.
Na drugim biegunie diety znajdują się ludzie Hadza — jedno z ostatnich plemion zbieracko-łowieckich w Tanzanii. W 2017 roku Samuel Smits, Justin Sonnenburg i współpracownicy ze Stanforda opublikowali w Science analizę 350 próbek kału zebranych od członków tego plemienia przez ponad rok. Mikrobiota Hadza okazała się zdecydowanie bardziej zróżnicowana niż mikrobiota mieszkańców krajów uprzemysłowionych i wykazywała wyraźną cykliczność sezonową — więcej bakterii rozkładających błonnik w porze suchej, odmienny profil w porze deszczowej, co odpowiadało zróżnicowanemu pożywieniu w tych okresach. Pewne taksony bakteryjne znikały w jednym sezonie, by odrodzić się w następnym. W populacjach uprzemysłowionych te same taksony zanikły na stałe.
To obserwacja spójna z wcześniejszym badaniem Eriki i Justina Sonnenburgów, opublikowanym w Nature w 2016 roku. Na modelu mysim wykazali, że dieta uboga w błonnik przez cztery pokolenia prowadzi do nieodwracalnej utraty gatunków bakteryjnych — nawet po przywróceniu błonnika do diety pewne gatunki nie wracają. Sonnenburgowie nazwali to „wymieraniem gatunkowym" w obrębie mikrobiomu.
Przez dekady dietetyka opierała się na prostym założeniu: ten sam posiłek powinien działać na wszystkich ludzi mniej więcej tak samo. Indeks glikemiczny — skala porównująca, jak szybko dany produkt podnosi poziom cukru we krwi — stał się jednym z filarów zaleceń żywieniowych dla diabetyków i osób z nadwagą. Problem w tym, że indeks ten oparty jest na uśrednionych reakcjach dużych grup ludzi. A co, jeśli to uśrednianie ukrywa więcej, niż pokazuje?
W 2015 roku zespół Erana Segala i Erana Elinava z Instytutu Weizmanna opublikował w Cell badanie, które postawiło tę kwestię na ostrzu noża. Przez tydzień monitorowali w trybie ciągłym poziom glukozy u 800 osób, rejestrując reakcje poposiłkowe na prawie 47 tysięcy posiłków. Odkryli, że odpowiedź glikemiczna na identyczny posiłek różniła się między poszczególnymi osobami dramatycznie. Jeden uczestnik mógł zjeść banan i doświadczyć gwałtownego skoku cukru, podczas gdy u innego ten sam banan ledwie poruszał igłą glukometru. Za to sushi — pozornie „lekkie" — u niektórych osób wywoływało reakcję glikemiczną porównywalną ze zjedzeniem czekoladowego batona. Koniec z uniwersalnym „to jest zdrowe, a to nie". Zależy dla kogo.
Kluczowe okazało się to, że algorytm uczenia maszynowego, uwzględniający skład mikrobioty jelitowej, parametry krwi, nawyki żywieniowe i aktywność fizyczną, potrafił przewidywać indywidualne reakcje glikemiczne z dokładnością niedostępną dla tradycyjnych metod. Personalizowane diety zaprojektowane na podstawie tego algorytmu skutecznie obniżały poposiłkowe szczyty glukozowe u uczestników.
Badanie Segala i Elinava nie było pozbawione krytyki — kwestionowano między innymi rolę zmienności wewnątrzosobniczej w pomiarach — ale otworzyło drogę do zupełnie nowego myślenia o żywieniu. Diety przyszłości mogą być projektowane nie dla populacji, lecz dla konkretnego człowieka, z uwzględnieniem składu jego osobistego ekosystemu bakteryjnego.
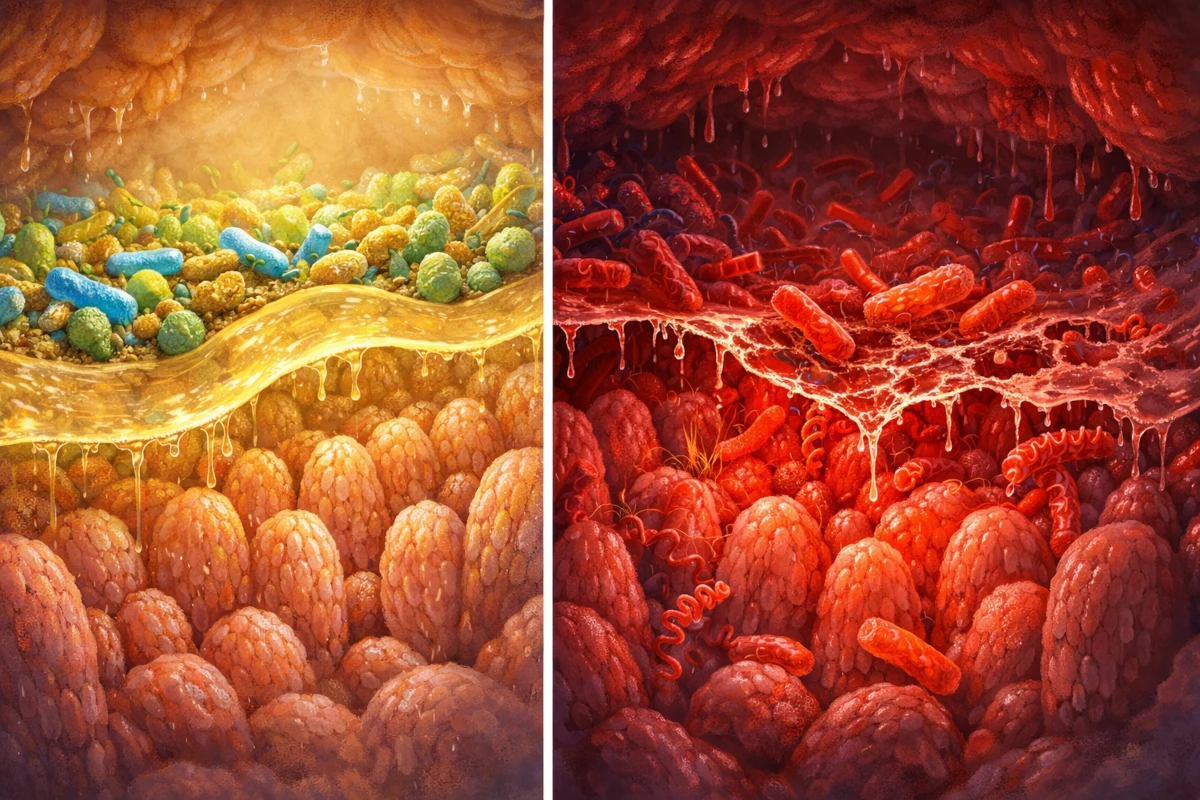
Wizualizacja AI / faleinspiracji.pl / CC BY 4.0
Probiotyki: nadzieja, rynek i rozczarowanie
Siedemdziesiąt miliardów dolarów. Tyle, według niektórych prognoz, będzie wart globalny rynek probiotyków do końca tej dekady.
A teraz pytanie, które powinnam zadać znacznie wcześniej: ile z tego ma pokrycie w twardych dowodach klinicznych? Mniej, niż sugerują opakowania w aptece. Problem polega na tym, że większość komercyjnych probiotyków opiera się na szczepach wybranych nie dlatego, że mają najsilniejsze działanie zdrowotne, ale dlatego, że łatwo je hodować, pakować i przechowywać. Gatunki Lactobacillus i Bifidobacterium dominują na półkach nie ze względu na swoją terapeutyczną wyższość, lecz z powodu technologicznej wygody — dobrze znoszą warunki tlenowe, przeżywają w kapsułkach i na liście suplementów mają wieloletnią historię bezpieczeństwa.
Tyle że te bakterie, choć bezpieczne i czasem korzystne, są w jelitach raczej turystami niż rezydentami. Większość komercyjnych szczepów po zażyciu przechodzi przez przewód pokarmowy i znika w ciągu kilku dni, nie kolonizując trwale jelita. Rdzenną mikrobiotę, ukształtowaną we wczesnym dzieciństwie i w znacznym stopniu stabilną przez resztę życia, trudno jest trwale zmienić garstką kapsułek z supermarketu.
Dlatego nauka coraz wyraźniej odwraca się ku zupełnie innej klasie preparatów — tzw. probiotykom nowej generacji (NGP). Chodzi o szczepy beztlenowców, które naturalnie zamieszkują ludzkie jelita i pełnią w nich kluczowe funkcje, ale do niedawna były nie do okiełznania technologicznie. Dwa gatunki budzą największe nadzieje.
Pierwszy to Akkermansia muciniphila — bakteria żyjąca w warstwie śluzu jelitowego. W badaniach na ludziach wykazano, że jej podaż (co ciekawe, również w formie pasteryzowanej, nieżywej) poprawiała wrażliwość na insulinę i markery metaboliczne u osób z nadwagą i insulinoopornością. Akkermansia stała się swego rodzaju ikoną badań nad metabolizmem; jej niedobór obserwuje się konsekwentnie u pacjentów z cukrzycą typu 2 i otyłością.
Drugi to Faecalibacterium prausnitzii — jeden z najobficiej reprezentowanych gatunków w zdrowym jelicie grubym i zarazem potężny producent maślanu. Jego niedobór jest jednym z najbardziej powtarzalnych markerów dysbioz towarzyszących nieswoistym zapaleniom jelit, zwłaszcza chorobie Leśniowskiego-Crohna. Trwają próby kliniczne z preparatami opartymi na tym gatunku (np. EXL01), ale bezwzględna beztlenowość F. prausnitzii czyni jego produkcję farmaceutyczną poważnym wyzwaniem inżynieryjnym — bakteria ginie w kontakcie z tlenem, co komplikuje każdy etap od hodowli po pakowanie.
Bakterie programowane jak oprogramowanie
Wyobraź sobie kapsułkę, w której zamiast leku siedzi bakteria. Połykasz ją, bakteria dociera do jelita i czeka. Nic nie robi, dopóki nie wyczuje czegoś konkretnego — powiedzmy, podwyższonego stężenia tlenku azotu, markera stanu zapalnego. Dopiero wtedy włącza się jej obwód genetyczny i bakteria zaczyna lokalnie wydzielać substancję przeciwzapalną. Precyzyjnie tam, gdzie jest potrzebna. Tylko wtedy, gdy jest potrzebna.
To nie jest abstrakcyjna wizja. To kierunek badań nad tzw. inżynieryjnymi żywymi produktami bioterapeutycznymi — w angielskiej terminologii Engineered Live Biotherapeutic Products (eLBP). Zamiast podawać pacjentowi lek systemowy krążący po całym organizmie, wprowadza się do jelita genetycznie zmodyfikowaną bakterię zaprogramowaną na wykonanie ściśle określonego zadania. Bez obciążania organizmu sterydami, bez zastrzyków, bez efektów ubocznych typowych dla terapii ogólnoustrojowych.
Równolegle rozwijana jest terapia fagowa wspomagana narzędziami CRISPR-Cas9. Bakteriofagi to wirusy atakujące wyłącznie bakterie — każdy typ faga rozpoznaje ściśle określone gatunki lub nawet szczepy. Łącząc naturalną specyficzność fagów z inżynierią genetyczną CRISPR, naukowcy tworzą swego rodzaju „naprowadzane pociski", zdolne eliminować konkretne patogeny bez naruszania reszty mikrobioty. To podejście budzi nadzieję zwłaszcza w kontekście narastającej antybiotykooporności — jednego z najpoważniejszych zagrożeń zdrowia publicznego XXI wieku. Wielolekooporne szczepy Pseudomonas aeruginosa u pacjentów z mukowiscydozą czy oporne na wankomycynę Clostridioides difficile to cele, wobec których tradycyjne antybiotyki coraz częściej okazują się bezsilne.
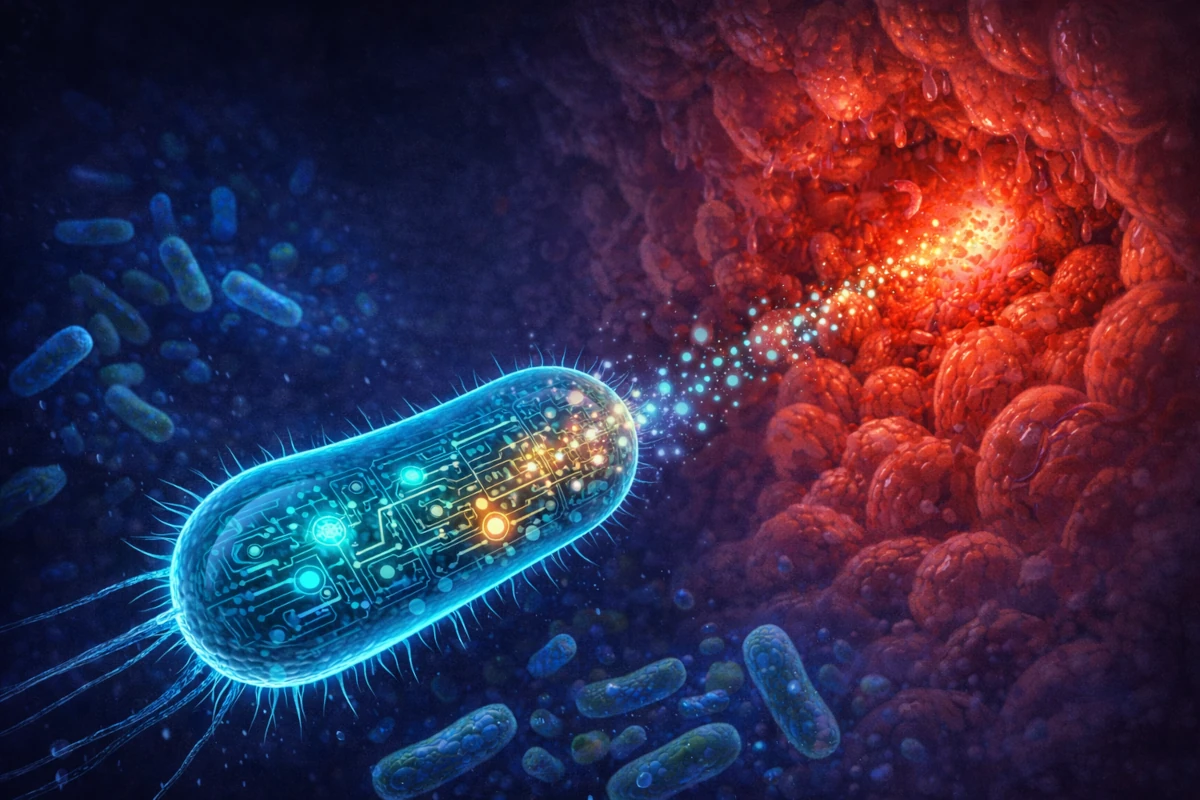
Wizualizacja AI / faleinspiracji.pl / CC BY 4.0
Transplantacja, która ratuje życie
To będzie krótko, bo zabrzmi niesmakowicie: transplantacja mikrobioty kałowej (FMT) polega na przeniesieniu zawiesiny mikroorganizmów z kału zdrowego dawcy do jelita biorcy.
I działa fenomenalnie. W przypadku nawracających zakażeń Clostridioides difficile — bakterii wywołującej ciężkie, potencjalnie śmiertelne zapalenie jelita grubego — FMT osiąga skuteczność rzędu 80–90%, przewyższając wielokrotne kursy antybiotyków.
W Polsce procedury FMT są dostępne w wyspecjalizowanych ośrodkach, a Polskie Towarzystwo Gastroenterologii (PTG-E) opracowuje wytyczne dotyczące kwalifikacji dawców i biorców. Kwalifikacja dawcy to proces rygorystyczny — wyklucza się osoby z chorobami zapalnymi jelit, zaburzeniami metabolicznymi, chorobami psychicznymi i wieloma innymi stanami, ponieważ wraz z bakteriami przenoszone jest całe spektrum cech ekosystemowych, których konsekwencji nie zawsze potrafimy przewidzieć.
To nie jest koniec, to jest początek
Kiedy Antonie van Leeuwenhoek w 1683 roku po raz pierwszy obserwował przez swój prymitywny mikroskop „animalcules" — drobne stworzonka krzątające się w osadzie z własnych zębów — nie mógł wiedzieć, że patrzy na fragment ekosystemu decydującego o zdrowiu i chorobie każdego z nas. Od tamtego momentu do pierwszych pełnych sekwencji metagenomowych mikrobiomu upłynęło ponad trzysta lat.
Dziś wiemy, że nasz mikrobiom to coś więcej niż zbiór pasażerów na gapę. To funkcjonalny organ o masie porównywalnej z mózgiem, produkujący setki metabolitów, regulujący odporność, współdecydujący o naszym nastroju. Coraz jaśniejsze staje się też, że bakterie jelitowe wpływają na skuteczność przyjmowanych leków. Klasyczny przykład: Eggerthella lenta, niepozorny beztlenowiec, potrafi dezaktywować digoksynę — lek stosowany w niewydolności serca — redukując ją do nieaktywnej dihydrodigoksyny. Bakteryjne beta-glukuronidazy z kolei mogą reaktywować w jelicie metabolity irynotekan — leku przeciwnowotworowego — powodując ciężkie, toksyczne biegunki. Farmakomikrobiomika, czyli nauka o interakcjach między lekami a mikrobiotą, to jedno z najszybciej rozwijających się pól badawczych współczesnej medycyny.
Wiemy też, że ten organ jest kruchy. Antybiotyki, diety ubogie w błonnik, sterylne warunki wychowywania dzieci, cesarskie cięcia bez odpowiedniej kompensacji probiotycznej — to wszystko go osłabia, a konsekwencje ujawniają się latami.
Nie jesteśmy jednak bezradni. Badania nad probiotykami nowej generacji, terapiami fagowymi, inżynieryjnymi bioterapeutykami i spersonalizowanym żywieniem opartym na profilu mikrobioty otwierają perspektywy, które jeszcze dekadę temu wydawały się odległe. Nauka o mikrobiomie nie obiecuje cudownych pigułek — raczej zmianę optyki. Zdrowia nie da się zrozumieć, patrząc wyłącznie na ludzkie komórki, ludzkie geny, ludzki organizm jako zamknięty układ.
Następnym razem, gdy będziecie sięgać po jogurt naturalny albo zastanawiać się, czy dorzucić do obiadu porcję kiszonej kapusty — wiedzcie, że nie karmicie tylko siebie. Karmicie też 38 bilionów współlokatorów, z którymi dzielicie każdy centymetr przewodu pokarmowego. I którzy, jak się okazuje, mają całkiem sporo do powiedzenia w kwestii waszego zdrowia.
Literatura i źródła
- Sender R., Fuchs S., Milo R., „Revised Estimates for the Number of Human and Bacteria Cells in the Body", PLOS Biology, 2016 artykuł naukowy
- Zeevi D., Korem T., Zmora N. i in., „Personalized Nutrition by Prediction of Glycemic Responses", Cell, 163(5), 2015 artykuł naukowy
- Desai M.S., Seekatz A.M., Koropatkin N.M. i in., „A Dietary Fiber-Deprived Gut Microbiota Degrades the Colonic Mucus Barrier and Enhances Pathogen Susceptibility", Cell, 167(5), 2016 artykuł naukowy
- Messaoudi M., Lalonde R., Violle N. i in., „Assessment of psychotropic-like properties of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175) in rats and human subjects", British Journal of Nutrition, 105(5), 2011 artykuł naukowy – baza PubMed
- Messaoudi M., Violle N., Bisson J.F. i in., „Beneficial psychological effects of a probiotic formulation (Lactobacillus helveticus R0052 and Bifidobacterium longum R0175) in healthy human volunteers", Gut Microbes, 2(4), 2011 artykuł naukowy – wydawca komercyjny
- Vinderola G., Sanders M.E., Salminen S., „The Concept of Postbiotics", Foods, 11(8), 2022 artykuł naukowy – baza PubMed
- Swanson K.S., Gibson G.R. i in., „The International Scientific Association for Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of synbiotics", Nature Reviews Gastroenterology & Hepatology, 17, 2020 artykuł konsensusowy – czasopismo naukowe
- Clarke S.F. i in., „Exercise and associated dietary extremes impact on gut microbial diversity", Gut, 63(12), 2014 artykuł naukowy – baza PubMed
- Sonnenburg E.D., Smits S.A., Tikhonov M. i in., „Diet-induced extinctions in the gut microbiota compound over generations", Nature, 529, 2016 artykuł naukowy
- Smits S.A., Leach J., Sonnenburg E.D. i in., „Seasonal cycling in the gut microbiome of the Hadza hunter-gatherers of Tanzania", Science, 357(6353), 2017 artykuł naukowy
- Miecznikow I., The Prolongation of Life: Optimistic Studies, G.P. Putnam's Sons, 1907 monografia historyczna; opracowanie encyklopedyczne (Wikipedia)
- „Mikrobiom jelitowy", Wikipedia hasło encyklopedyczne
- Salminen S. i in., „The International Scientific Association of Probiotics and Prebiotics (ISAPP) consensus statement on the definition and scope of postbiotics", Nature Reviews Gastroenterology & Hepatology, 18, 2021 artykuł konsensusowy – czasopismo naukowe
- Canfora E.E., Jocken J.W., Blaak E.E., „Short-chain fatty acids in control of body weight and insulin sensitivity", Nature Reviews Endocrinology, 11, 2015 artykuł przeglądowy
- Cryan J.F., O'Riordan K.J. i in., „The Microbiota-Gut-Brain Axis", Physiological Reviews, 99(4), 2019 artykuł przeglądowy – baza PubMed
- Van Nood E. i in., „Duodenal Infusion of Donor Feces for Recurrent Clostridium difficile", New England Journal of Medicine, 368, 2013 artykuł kliniczny